ARDS je akutní forma postižení plicní tkáně, která vede k poruše funkce plic. Jedná se o častý problém pacientů v intenzivní péči. Přes to, že už je popsán od roku 1967 je i v dnešní době stále hodně poddiagnostikován. Jeho incidence se odhaduje na 7 až 85 případů na 100 000 hospitalizovaných pacientů v intenzivní péči. Některé studie pak ukázaly, že ARDS bylo přítomno až u 7% hospitalizovaných pacientů na jednotkách intenzivní péče.
Patofyziologie
Patofyziologie není zatím zcela objasněna. Nicméně mikroskopicky pozorujeme difuzní poškození alveolů a jejich zaplavení tekutinou bohatou na proteiny. Rovněž je pozorována přítomnost neutrophilů a ztráta epitelových buněk alveolů (apoptóza pneumocytů). Dále vidíme vznik hyalinových membrán u baze přítomných penumocytů a formující se mikrotromby v mikrocirkulaci.
Zaplavení alveolů vzniká na podkladě poškození alveolo- kapilární membrány a je hlavní determinantou ARDS. Alveolo kapilární membrána ztrácí svou integritu kvůli apoptoze pneumocytů, ke které dochází difuzně ve všech alveolech. Kapilární část membrány je tvořena endothelem, který se jeví více permeabilní. Díky zvýšené permeabilitě dochází k úniku tekutiny a také proteinů do alveolů a do intersticia. V průběhu času se edém zmenšuje a problémem se stává fibrosa (fibroproliferativní proces je někdy popisován již v počátcích).
Migrace neutrophilů do alveolů vede k amplifikaci zánětlivé odpovědi. Neutrophily produkují prozánětlivé markery, které vedou poté k apoptoze pneumocytů a prohloubení poškození alveolo- kapilární membrány.
Dalším problémem je disfunkce surfaktantu. K té dochází zejména kvůli zaplavení alveolů tekutinou bohatou na proteiny. Tím se naruší povrchové napětí vytvořené surfaktantem. To vede ke kolabování alveolů při výdechu a je zapotřebí mnohem větší usílí ke znovurozepnutí a nádechu.
Zároveň dochází vlivem poruchy koagulace k tvorbě mikrotrombů v kapilární části plicního řečiště. Dochází k rozvoji plicních zkratů vlivem zvýšenému nepoměru mezi ventilací a perfuzí plic. K vzniku mikrotrombů nedochází pouze v plicích, ale i ve všech ostatních orgánech.
- Disfunkce alveolo – kapilární membrány
- apoptóza pneumocytů
- zvýšená permeabilita kapilární části membrány
- Zaplavení alveolů tekutinou bohatou na proteiny (plicní edém bohatý na proteiny)
- Migrace neutrophilů do alveolů
- Disfunkce surfaktantu
- Vznik mikrotrombů
Rizikové faktory
ARDS téměř vždy vzniká na podkladě rizikových faktorů. Pravděpodobnost vzniku ARDS stoupá s přítomnými více rizikovými faktory.
Drtivá většina pacientů má systémové onemocnění, se zánětlivou aktivitou a orgánovou dysfunkcí mimo plíce.
Hlavním rizikovým faktorem je tedy sepse. Riziko vzniku ARDS u sepse je popisováno až 30%. Riziko zvyšuje rovněž místo odkud sepse vzniká. U pacientů kde je původem pneumonie je riziko zvýšeno. Dalším známým rizikem je trauma, spojené s crush syndromem a masivními krevními náhradami. Mezi minoritní rizikové faktory pak patří nikotinismus, obezita, stav po resekci plic. Naopak se ukázalo, že pacienti s diabetes mellitus mají nižší prevalenci k ARDS.
- Sepse -> zejména pokud je zdrojem pneumonie
- Trauma -> spojené s crush syndromem a masivními krevními převody
- Nikotinismus, obezita, stav po resekci plic
Diagnostika
Dnes definujeme ARDS dle Berlínské definice. Ta již nepoužívá termín Acute Lung Injury (ALI) ale pouze ARDS s dělí ho na mírné, střední a těžké. Stupeň tíže je založen zejména na míře hypoxie – Horowitzově indexu.
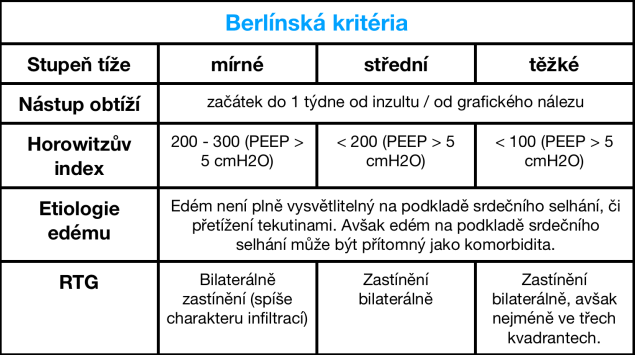
Rozlišení edému na podkladě ARDS a na podkladě srdečního selhání může být v praxi obtížné a předpokládá se i částečný překryv obou diagnóz (edém na podkladě ARDS a hydrostatický edém).
Diagnózu ARDS většinou stanovujeme klinicky a na podkladě RTG snímku. Druhou nejpoužívanější metodou je bronchoskopie, která ale není ke stanovení diagnózy nutná a často její rizika převyšují benefit. Jedinou výhodou je možnost stanovení původce penumonie a mířit tak antibiotickou léčbu cíleně dle kultivace. V minulosti byla rovněž prováděna biopsie plic.
Klinické projevy
ARDS můžeme rozdělit dle klinických projevů na počáteční fázi, pozdní fibroproliferativní fázi a fázi hojení.
- počáteční fáze
- fibroproliferativní fáze
- fáze hojení
Počáteční fáze
Počáteční fáze se projevují zejména rozvojem zastínění na RTG snímku plic, hypoxémií, edémem plic a zvýšenou dechovou prací. Na CT (které se běžně v praxi nepoúžívá) jsou popisovány okrskovité atelektázy a edém alveolů. Hypoxémie, která je zpočátku onemocnění přítomna dobře odpovídá na zvýšení frakce kyslíku. Zvýšená dechová práce je důsledkem snížené plicní compliance a zvýšenému odporu při proudění vzduchu. Snížení dechové práce docílíme pomocí umělé plicní ventilace (u některých pacientů postačí NIV nebo HFNO). Kvůli hypoxemii a zvýšené dechové práci dochází u většiny pacientů (až 92%) k rozvoji plicní hypertenze (fyziologicky se organismus plicní vazokonstrikcí snaží omezit perfuzi alveolů, které nejsou dostatečně ventilované) a následně k pravostrannému srdečnímu selhávání.
- hypoxémie
- zvýšená dechová práce
- plicní hypertenze a selhávání pravého srdce
Fibroproliferativní fáze
Tato fáze navazuje na fázi počáteční. U většiny pacientů dochází vlivem zánětlivé reakce k fibrosní alveolitidě. Dochází k fibrózní přestavbě plicní tkáně. Tato fáze obvykle nastává po 7 – 10 dnech od počátku onemocnění (ukládání hyalinu subepitheliálně je však patrné od počátku onemocnění, nemá však klinický korelát). V této fázi dochází k vyplnění alveolů a mezialveolárních sept hyalinem, fibronsí tkání a novými kapilárami. Plicní compliance se dále snižuje a zapotřebí stále umělá plicní ventilace. Zároveň dochází k potřebě navýšení frakce kyslíku a navýšení PEEP. pacienti v této fázi velmi špatně odpovídají na recruitment manevr. Tato fáze je velmi často komplikována ventilátorovou pneumonií a jinými nozokomiálními infekcemi. Studie ukazují, že incidence této fáze klesá s používáním protokolu LTVV (low tidal volume ventilation).
- ukládání hyalinu (od počátku onemocnění)
- klinické projevy 7 – 10 dní od počátku onemocnění
- fibrosní přestavba, neovaskularizace
Fáze hojení
Biopsie plicní tkáně odebrané přeživším pacientům jsou téměř bez patologického nálezu. Během hojení tedy musí docházet ke vstřebání edému alveolů a proteiny musí být odstraněny extracelulární cestou intersticiem plicní tkáně. Zároveň musí dojít k obnově alveolárního epithelu. Některé studie prokazují, že neutrophily, které migrovali do alveolů v konečné fázi podstupují apoptózu a hojně mizí. Poslední fází, která musí během hojení proběhnout je remodelace plicní tkáně a její přestavba do původního charakteru. Tyto procesy trvají řádově několik měsíců, během kterých se postupně navrací i funkce plic. Zvyšuje se jak ventilační tak oxygenační parametry a postupně se nsižuje dechová práce.
- upravení do původního stavu
- fáze probíhá několik měsíců, během kterých se upravují rovněž plicní funkce
Léčba
Kauzální léčba bohužel není. Proto se léčba zaměřuje na prevenci a na podporu vitálních funkcí během onemocnění.
Hlavním problémem je respirační selhání a nutnost zahájení umělé plicní ventilace. Zároveň se jedná o hlavní část symptomatické léčby. Více o ventilační strategii u pacientů s ARDS naleznete zde.
Léčba rizikových faktorů dává největší důraz na penumonii a sepsi. Včasné zahájení léčby u sepse je proto velmi důležité, v prevenci vzniku ARDS.
Dlouhodobě se debatuje o tom, jakou zvolit strategii volumoterapie. V principu jsou dva přístupy. Liberální přístup argumentuje udržením dostatečného intravaskulárního objemu a zlepšení perfuze cílových orgánů, protože většina pacientů umírá na komplikace ARDS a poškození jiných orgánových funkcí. Restriktivní přístup naopak dává do popředí snížení intravaskulární náplně a tedy snížení drivu, kterým vzniká plicní edém. Studie neprokázali významný klinický rozdíl mezi oběma skupinami pacientů. Nicméně se doporučuje cílit na co nejmenší náplň intravaskulárního prostoru při zachovalé dobré perfuzi cílových orgánů.
Dalším velmi zkoumaným tématem byla nutrice pacientů s ARDS. Ukázalo se, že nejvýhodnější strategií je enterální výživa s vysokým obsahem tuků a sníženým obsahem bílkovin. Docílíme tak snížené nálože dusíku. U takto živených pacientů poté bylo detekováno zkrácení doby kdy u nich bylo nutné použít umělou plicní ventilaci. Zároveň bychom se u všech pacientů s ARDS měli vyvarovat overfeedingu.
U pacientů, kteří neodpovídají na běžně zavedenou léčbu je dnes používána pronační poloha. Ukázalo se, že pronační poloha zlepší oxygenační funkci plic. Dnes je pronační poloha stále častěji používána i u pacientů se středně závažným ARDS. Obecně dnes platí indikace k pronační poloze Horowitzův index pod 150. Dalším stupněm léčby u těchto pacientů je napojení na ECMO (extracorporeal membrane oxygenation). Užití vysokofekveční oscilační ventilace neukázalo žádný benefit a mělo by být použito pouze jako ultimum refugium. Za zvážení také stojí podání inhalačně oxidu dusného a prostacyklinu, jako dobrých bronchodilatátorů, nicméně ani toto není rutinně používáno.
- včasná léčba infekce / pneumonie / sepse -> hledat patogen
- snížení dechové práce pomocí UPV / NIV / HFNO
- volumoterapie s cílem co nejnižší náplně řečiště při dobré perfuzi orgánů
- vyvavorovat se overfeedingu, preferovat dietu s vyoským obsahem tuků a nízkou náloží bílkovin
